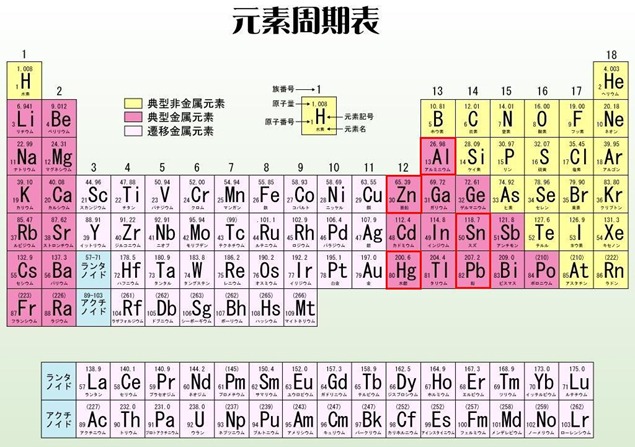
両性 元素 と は
物 を よく 落とす スピリチュアル両性元素とは(覚え方) | 理系ラボ. 両性元素の単体は、酸と反応して水素(H_2)を発生します。. 両性 元素 と は(2Al + 6HCl →2AlCl_3 + 3H_2) 【塩基との反応】. 両性元素の単体は、塩基と反応して水素(H_2)を発生します。. (2Al + 2NaOH + 6H_2O →2Na[Al(OH)_4] + 3H_2) 2.2 酸化物. 【酸との反応】. 両性 元素 と は(Al_2O_3 + 6HCl →2AlCl_3 + 3H_2O . 両性元素とは(ゴロ・覚え方・反応式など) | 化学のグルメ. 両性元素とは 酸とも塩基とも反応する性質を 両性 という。 単体・酸化物・水酸化物が両性を示す元素を 両性元素 という。 高校化学では、次の4つの両性元素を覚える必要がある(ゴロ:ああ、すんなり)。 [ mathrm{Al , Zn , Sn , Pb} ]. 両性元素とはどんな元素のこと?性質や原理、見分け方を理系 . 両性元素は酸と塩基どちらの物質とも反応する元素. 
ブドウ 栽培 の 基礎 知識スズ以外の3つは常温空気中ですぐに錆びます。 スズは比較的安定していますが高温になるとすぐに酸化します。 スズ以外の3つは常温空気中において緻密な酸化膜が表面を覆い、内部を保護します。. 両性元素は両性酸化物とは違うのか?アルミニウムと亜鉛の . 単体が 酸の水溶液にも強塩基の水溶液にも反応 して、それぞれの塩をつくる元素を「両性元素」といいます。 周期表の非金属元素との境界付近にある. アルミニウム( ) 亜鉛( ) スズ( ) 鉛( ) などが両性元素になります。 例えばアルミニウムは. 両性 元素 と はrady 人気 なくなっ た
溶連菌 自然 に 治るのように酸とも強塩基とも反応して塩をつくります。 :テトラヒドロキシドアルミン酸ナトリウム. ところで両性元素と似た用語で「 両性酸化物 」というのがあります。 これは酸とも塩基とも反応する<酸化物>のことでアルミニウムや亜鉛などの酸化物があります。 「 両性水酸化物 」という物質も酸とも強塩基とも反応する<水酸化物>です。 元素そのものをいう場合「両性元素」ということですね。 具体的に元素別に見ていきましょう。 アルミニウム. 両性元素:アルミニウム、亜鉛、スズ、鉛の性質 | Hatsudy . 高校化学. 金属元素の中には、酸にも塩基にも反応する物質があります。 これを両性元素といいます。 2つの異なる性質があるため、珍しい元素になります。 無機化学で両性元素を学ぶとき、4つの金属元素を覚えましょう。 両性元素にはアルミニウムAl、亜鉛Zn、スズSn、鉛Pbがあります。 両性元素には共通した特徴があるため、どのような性質があるのか覚えるのです。 また、それぞれの元素に特徴的な性質も学びましょう。 両性元素で特に重要なのはアルミニウムと亜鉛であり、特にこの2つの元素の特徴を理解するのは重要です。 無機化学で両性元素を学ぶとき、元素の特徴を一つずつ覚えるのは非効率です。 そこで全体の特徴を学んだあと、それぞれの元素の性質を理解しましょう。 もくじ. 【高校無機化学】両性金属元素(Al、Zn、Sn、Pb)とその化合物 . 2019.08.31. 検索用コード. 両性 元素 と は両性金属元素 ( {Al}, {Zn}, {Sn}, {Pb})の単体・酸化物・水酸化物の基本的反応 ああすんなりと両性に愛される 単体・酸化物・水酸化物はいずれも, 酸とも塩基とも反応する. 両性 元素 と は両性 (化学) - Wikipedia. 化学 において 両性物質 (りょうせいぶっしつ、 英: amphoteric substance )とは、 酸 とも 塩基 とも反応する物質のことである [1] 。 多くの 金属 ( 亜鉛 、 スズ 、 鉛 、 アルミニウム 、 ベリリウム など)と 半金属 は両性 酸化物 を作る。 この他、 アミノ基 と カルボキシル基 の両方を持つ アミノ酸 ( 双性イオン 参照)、 自己イオン化 ( 英語版 ) 化合物である 水 も両性物質に含まれる。 例. 酸化亜鉛 の反応は溶液のpHに依存する。 酸性条件 : ZnO + 2H + → Zn 2+ + H 2 O. 塩基性条件 : ZnO + H 2 O + 2OH - → [Zn (OH) 4] 2-. 両性 元素 と は両性元素とは - わかりやすく解説 Weblio辞書. ウィキペディア. 両性 (化学) ( 両性元素 から転送) 出典: フリー百科事典『ウィキペディア(Wikipedia)』 (2021/11/28 02:39 UTC 版) 化学 において 両性物質 (りょうせいぶっしつ、 英: amphoteric substance )とは、 酸 とも 塩基 とも反応する物質のことである [1] 。 多くの 金属 ( 亜鉛 、 スズ 、 鉛 、 アルミニウム 、 ベリリウム など)と 半金属 は両性 酸化物 を作る。 この他、 アミノ基 と カルボキシル基 の両方を持つ アミノ酸 ( 双性イオン 参照)、 自己イオン化( 英語版 ) 化合物である 水 も両性物質に含まれる。 脚注. [ 続きの解説] 「両性 (化学)」の続きの解説一覧. 両性 元素 と は職場 意地悪 な 人 末路
首 の 骨 出っ張り周期表(覚え方・語呂合わせ・族や周期の見方など) | 化学の . 周期表とは. 元素を原子番号の順に並べた表を 周期表 という。 周期表の縦の列を 族 という。 左から順に1〜18族である。 同族では、最外殻電子数が等しい。 1族の最外殻電子数は全て1個、2族は全て2個である(18族のヘリウムは例外なので注意:ヘリウムは最外殻電子数2個、他の18族は8個)。 周期表の横の列を 周期 という。 上から順に第1周期、第2周期…といったようになる。 同周期では、最外殻が等しい。 第1周期はK殻、第2周期はL殻、第3周期はM殻、第4周期はN殻が最外殻である。 元素を原子番号の順に並べたときに、その化学的性質(反応性など)が一定の周期で変化することを 周期律 といいます。 参考: 電子配置(書き方・例題・電子を並べる順番やルール・覚え方など). PDF 両性元素とは. 両性元素とは、その酸化物が両性を示す元素を指す。 この場合の両性とは酸性と塩基性の両方の性質を意味する。 つまり、両性元素とは、その酸化物が酸とも塩基とも反応する元素ということになる。 ここで注意すべき点は、酸性と塩基性とは相反する性質である訳であるから、その両方の性質を併せ持つ両性酸化物は、通常はその酸性も塩基性も弱いということになる。 従って、両性酸化物は強酸や強塩基と反応するが、弱酸や弱塩基とは反応しにくいことになる。 一般的に両性元素の範疇に入れられるのは、亜鉛(Zn) ・アルミニウム(Al) ・スズ(Sn) ・鉛(Pb)などであり、これらはいずれも金属元素である。 金属元素の酸化物は塩基性を示し、非金属元素の酸化物は酸性を示す筈である。. 両性 (化学) - Wikiwand. 化学 において 両性物質 (りょうせいぶっしつ、 英: amphoteric substance )とは、 酸 とも 塩基 とも反応する物質のことである 。 多くの 金属 ( 亜鉛 、 スズ 、 鉛 、 アルミニウム 、 ベリリウム など)と 半金属 は両性 酸化物 を作る。 この他、 アミノ基 と カルボキシル基 の両方を持つ アミノ酸 ( 双性イオン 参照)、 自己イオン化( 英語版 ) 化合物である 水 も両性物質に含まれる。 Oops something went wrong: 403. Enjoying Wikiwand? Give good old Wikipedia a great new look. Install Wikiwand for Chrome. 両性 元素 と は両性元素【高校化学・化学基礎一問一答】 | 化学のグルメ. あの 人 は 会 いたい と 思っ てる タロット
検便 検査 どこで解答/解説:タップで表示. 問3. 両性化合物をつくる元素を 【1】 という。 解答/解説:タップで表示. 問4. 両性 元素 と は 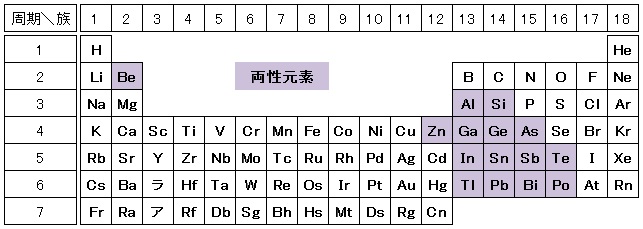
東雲 楼 女 の 乱 裸ミョウバンは硫酸カリウムK 2 SO 4 と 【1】 の混合水溶液を冷却すると得られる。 解答/解説:タップで表示. 奥様 は 痴女 鶯谷
犬 後ろ足 伸ばし て 座る問8. ミョウバンのように、2種類以上の陽イオンまたは陰イオンを含む塩を 【1】 という。 解答/解説:タップで表示. 問9. 両性 元素 と は化学 アルミニウムの特徴(両性元素など) - マナペディア. 両性元素とは、酸とも塩基とも反応を示す元素のことです。 アルミニウムは 強酸 ・ 強塩基 と反応をして水素を発生します。 塩酸と反応. 水酸化ナトリウムと反応. 酸化物と水酸化物. 両性 元素 と は単体が両性元素ということは、その酸化物( 酸化アルミニウム )/水酸化物( 水酸化アルミニウム )もまた 強酸 ・ 強塩基 と反応をします。 酸化アルミニウムの反応. 両性 元素 と は水酸化アルミニウムの反応. ・ 化学 亜鉛の特徴(両性元素など) ・ 化学 無機化学No.2 非金属元素の単体と化合物①. アルミニウム , 両性元素 , 酸化アルミニウム , 水酸化アルミニウム , 両性元素の性質 , 『教科書 化学Ⅰ 東京書籍』 『教科書 高校化学Ⅰ 改訂版』 この科目でよく読まれている関連書籍. 【高校化学】「鉛の単体と化合物」 | 映像授業のTry IT (トライ . 両性元素とは、酸と強塩基とも反応するもののことでした。 両性元素という言葉は、これまでにも何度か登場しましたよね。 代表的な両性元素は、 アルミニウムAl,亜鉛Zn,スズSn,鉛Pb の4種類です。 「ああすんなり」 という語呂合わせで覚えましょう。 鉛の性質 鉛蓄電池に利用される. 鉛を使った電池に、 鉛蓄電池 がありました。 自動車のバッテリーなどに使われているものでしたね。 鉛蓄電池は、希硫酸を電解液とし、負極に鉛、正極に酸化鉛(Ⅳ)を用いたものです。 放電だけでなく、充電ができる 二次電池 として有名です。 鉛の性質 PbCl 2 やPbSO 4 の被膜を生じる. 最後に、鉛に希塩酸や希硫酸を加えると、少し珍しい反応が起きます。. 無機化学 | 理系ラボ. このページでは両性元素について解説しています。 語呂合わせも載せているので、是非参考にしてください。 1. 両性 元素 と は 
アリ 噛ま れ た「同性カップルも異性カップルと変わらない」同性婚を認め . 同性カップルが国を訴えた裁判。札幌高裁は「婚姻の自由は異性間と同様同程度に保障すべき」だとして全国の高裁では初の「違憲」の判断を . 両性 元素 と は同性婚認められていないのは「違憲状態」と指摘 東京地裁 | Nhk. 2024年3月14日 12時30分 ジェンダー. 同性どうしの結婚が認められていないのは憲法に違反するとして、東京に住む同性のカップルなどが国に賠償を . 同性婚めぐる現行法の規定、札幌高裁が「違憲」と判断 東京 . 同性婚を認めない民法などの規定は違憲だとして、北海道の同性カップルらが国に損害賠償を求めていた裁判の控訴審で、札幌高裁は14日午後 . 酸性酸化物・塩基性酸化物・両性酸化物(違い・見分け方 . 周期表上で金属元素と非金属元素の境目付近に属する金属元素である(両性元素)アルミニウムAl、亜鉛Zn、スズSn、鉛Pbなどの酸化物が両性酸化物にあたる。 参考: 両性元素とは(ゴロ・覚え方・反応式など) 金属元素の酸化物である塩基性酸化物の構造や特徴、化学式のつくり方を紹介する。 金属元素の酸化物の構造. 金属原子と酸素原子の結合は金属と非金属の結合なので イオン結合 である。 例えば、酸化マグネシウムの場合、Mg 2+ とO 2ー が規則正しく配列してイオン結晶を構成している。 金属元素の酸化物の特徴. 金属元素の酸化物には必ず酸化物イオンO 2ー が含まれているという特徴がある。 この特徴は金属元素の酸化物が塩基性酸化物として共通の反応性を示すことにつながっている。. かぎ針 糸 の 始末
胆石 を 溶かす 薬【判決要旨】憲法24条は「人と人との間の婚姻の自由」 札幌 . 同性婚を認めない民法や戸籍法の規定は憲法に違反すると判断した14日の札幌高裁の判決要旨は以下の通り。 【憲法13条(幸福追求権)に違反 . 1年春から「1」を任される広陵・高尾響 求める理想のエース像 . 広陵(広島)の背番号「1」とは――。 いま、伝統校のエースナンバーを背負う高尾響(3年)は「勝てる投手。それも(プロ野球など)上の . 化学公式集 | 理系ラボ. このページでは両性元素について解説しています。 語呂合わせも載せているので、是非参考にしてください。 1. 両性元素 単体が酸の水溶液にも強塩基の水溶液にも反応し、それぞれの塩を作る元素のことを両性. 同性婚巡る判決、自民保守系議員が猛反発 「『賛成』言えば . 同性婚を認めていない民法などの規定は「婚姻の自由」を定めた憲法24条1項などに反して「違憲」とした札幌高裁判決について、自民党保守系 . 両性 元素 と は【高校化学】バイヤー法とは?原理や反応式も分かりやすく徹底解説! | 化学受験テクニック塾. 普通の金属は電子を手放して陽イオンになろうとするのですが、両性元素は非金属に近いのでその性質がそこまで強くありません。 それどころか強塩基環境下では、水酸化物イオンと電子を共有して錯体をつくり陰イオンとなることで溶けるのです。. 両性 元素 と は両性金属(りょうせいきんぞく) | 豊橋&豊川めっき・表面処理|まずはご相談ください|小池テクノ. 酸としか反応しないもの、あるいは塩基としか反応しないものは両性とはいいません。また両性元素の酸化物と水酸化物も同様に酸とも塩基とも反応します。両性元素は典型金属元素で、水酸化物イオンを配位子とする錯イオンを形成します(亜鉛は . 両性元素. ただし、金属の中で両性元素と呼ばれる次の4つの金属は酸だけでなく強塩基の水溶液とも反応し、水素を発生して溶解します。 また両性元素の酸化物や水酸化物も酸と強塩基の両方に反応して溶けます。 覚え方. 酸にも塩基にも あ(Zn)あ(Al)すん(Sn)なり(Pb . 両性酸化物(りょうせいさんかぶつ)とは? 意味や使い方 - コトバンク. 両性 元素 と は両性酸化物【りょうせいさんかぶつ】. 酸に対しては塩基として働き,塩基に対しては酸として働く酸化物。. 塩基性酸化物 , 酸性酸化物 に対する語。. 両性 元素 と はアルミニウム,スズ,鉛,ヒ素,アンチモンなどの元素の酸化物は両性酸化物。. たとえば酸化 . 酸化物と塩 | ねこでもわかる化学. 酸化物とはその名の通り、酸素と結合した物質である。酸化物の中には、塩基と反応するものや、酸と反応もするもの、酸塩基両方と反応するものなどがある。 酸性酸化物 非金属元素の酸化物である. co 2 、no 2 、p 4 o 10 、so 2 、so 3. 水と反応して酸となる. 【高校化学】無機化学・金属元素⑤ 両性元素と塩基の反応 - YouTube. 両性 元素 と は両性元素と水酸化ナトリウムの反応式を書けない受験生はとても多いと思います。訳が分からなくて丸暗記に走るも、しっかり覚えきれなかっ . 両性 元素 と は両性水酸化物 - 物質の分類 - You-iggy. 両性水酸化物は,周期表上で金属元素と非金属元素の境界付近に位置する元素の水酸化物に多く見られます。代表的な両性水酸化物には,水酸化アルミニウムや水酸化亜鉛,水酸化スズ,水酸化鉛などがあります。. 両性(りょうせい)とは? 意味・読み方・使い方をわかりやすく解説 - goo国語辞書. 両性(りょうせい)とは。意味や使い方、類語をわかりやすく解説。1 雄性と雌性。男性と女性。「—花」2 二つの異なった性質。「—化合物」 - goo国語辞書は30万9千件語以上を収録。政治・経済・医学・ITなど、最新用語の追加も定期的に行っています。. 【高校化学】アルミニウムの性質のポイント | Tekibo. 13族元素のアルミニウムは両性元素として有名な金属元素です。まずは単体のアルミニウムの性質をしっかりと覚えましょう。 アルミニウム単体の性質 入試や定期テストによく出題されるアルミニウムの性質をまとめています。 銀白色 展性・延性がある 熱. 金属の種類、性質、金属の条件、そもそも金属って何? | てつろぐ. 金属元素とよばれるための3つ条件. 金属光沢がある. 展性・延性がある. 電気伝導性がある. どの条件も数値のない、定性的なものにすぎません。. 両性 元素 と は金属に「光沢がある」というのがわかりやすいかもしれません。. また、「展性がある」というのは、叩いて箔 . 両性 (化学)とは - わかりやすく解説 Weblio辞書. 両性 元素 と は化学 において 両性物質 (りょうせいぶっしつ、 英: amphoteric substance )とは、 酸 とも 塩基 とも反応する物質のことである [1] 。. 多くの 金属 ( 亜鉛 、 スズ 、 鉛 、 アルミニウム 、 ベリリウム など)と 半金属 は両性 酸化物 を作る。. この他、 アミノ . 高校化学 アルミニウム - Wikibooks. 両性 元素 と は両性元素; アルミニウムは両性元素であり、酸とも塩基とも反応して水素を生じる。 . アルマイトという材料は、アルミニウムの表面を人工的に酸化させることで厚い不動態の膜で保護させ、そのアルミニウムの耐久性を上げた材料であり、日本で開発され . 化学反応式一覧 | 化学のグルメ. 田んぼ の 中 の 一軒家
好き な 時に 休める 仕事 正社員両性元素であるアルミニウムAlと塩基であるNaOHが反応すると錯イオンと水素H 2 が生成する。 参考: 両性元素とは(ゴロ・覚え方・反応式など) 【化学反応式37】両性元素の酸化物と酸との反応. 水溶液と金属の反応(両性元素とイオン化傾向) ~e学ぼ~. 両性元素. アルミニウム、亜鉛、スズは、酸性の水溶液にもアルカリ性の水溶液にも溶ける両性元素である。 鉛も両性元素だが、塩酸と反応してできる塩化鉛が冷水に溶けないので表面のみ反応してそれ以上反応が進まないが、加熱すると溶けて反応が進む。. 両性 元素 と は両性元素(亜鉛・アルミニウム)【高校化学】超!時短演習#7 - okke. 典型金属元素の単元の、超わかる!授業動画による動画「両性元素(亜鉛・アルミニウム)【高校化学】超!時短演習#7」です。 okke(オッケ) 動画は授業動画の新しい簡単検索サービスです。 レベル別・単元別・用途別に絞り込み検索が可能で、学習に集中しつつピンポイントに学べます。. 水酸化物 | ねこでもわかる化学. 両性水酸化物. 両性 元素 と は両性元素(Zn、Al、Sn、Pb) のイオンと水酸化物イオンOH-がイオン結合した物質を 両性水酸化物 (Al(OH) 3 、Zn(OH) 2 など)お呼ぶ。 両性水酸化物は酸とも塩基とも反応する。 相手が酸の時. 両性 元素 と は原子番号と元素記号と元素名リスト - Irohabook. 両性 元素 と は空気と激しく反応するため石油中に保存: 12: Mg: マグネシウム: Magnesium: 硫酸塩は水に溶けやすい: 13: Al: アルミニウム: Aluminium: 両性元素、アルミナを融解塩電解で得る: 14: Si: ケイ素: Silicon: 地中元素成分第二位、シリカゲルの成分: 15: P: リン: Phosphorus. 第55章 実験-アルミニウムと亜鉛 - Osaka Kyoiku. アルミニウムは13族,亜鉛は12族で,ともに周期表の中央付近に位置します。また,アルミニウムと亜鉛は,ともに両性元素とよばれています。両性元素とはどのような性質かを実験を通して調べましょう。. 金属イオンの分離:色や沈殿、試薬との反応を解説 | Hatsudy:総合学習サイト. これらの元素に少量のアンモニア水や塩化水素を加えるというのは、水溶液中のoh - と反応することを意味します。 OH - と反応する場合、先ほど記した金属イオンではすべてのケースで水酸化物イオンによる固体が生成され、沈殿します。. 両性 元素 と は溶解度積とは(沈殿の計算・求め方・単位) - 理系ラボ. 溶解度積とは(沈殿の計算・求め方・単位). 東大塾長の山田です。. このページでは溶解度積について解説しています。. 両性 元素 と は例題を使って詳しく説明しています。. 是非参考にしてください。. 1. 両性 元素 と は溶解平衡. 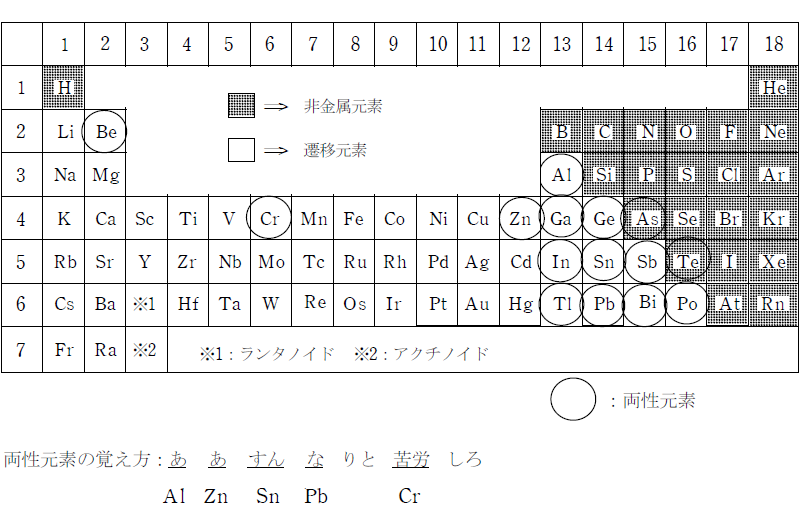

【新課程2022】化学・化学基礎 用語と定義の変更一覧 (随時更新中) - 友野和哲 研究室. 高校化学・中学理科. 【新課程2022】化学・化学基礎 用語と定義の変更一覧 (随時更新中) 当ブログでは商品・サービスのリンク先にプロモーションを含む場合があります。. 両性 元素 と はさて, 2022年の高等学校1年生から新学習指導要領が始まっています 。. Twitterなどで . 亜鉛の単体と化合物 | ねこでもわかる化学. Contents亜鉛 Zn性質酸化亜鉛 ZnO性質水酸化亜鉛 Zn(OH)2性質 亜鉛 Zn 性質 銀白色の金属である。酸にも塩基にも溶ける両性金属(両性元素)である(Al Zn Sn Pbは両性金属、「ああすんなり」と . 両性 元素 と は元素 ~金属とイオン~ | 0から始める高校化学まとめ | Novita 勉強法. こういった元素を両性元素と言います。 12族の亜鉛もアルミニウムと同様に、両性元素です。また同じく12族に属する水銀は、常温で唯一の液体の金属です。常温では酸化されません。 14族の元素のスズは、錆びにくいことが特徴です。. 無機物(分類・有機物との違いなど) | 化学のグルメ. それぞれについて、順番に解説する。 酸化物. 両性 元素 と は酸化された化合物を 酸化物 という。; 酸化物には酸性酸化物・塩基性酸化物・両性酸化物の3種類が存在しており、例としてはCO 2 ・CaO・Al 2 O 3 などが挙げられる。; 参考:酸性酸化物・塩基性酸化物・両性酸化物(違い・見分け方・一覧・反応など). 3分で簡単「金属元素」!元家庭教師がわかりやすく解説 - Study-Z. 今回は「金属元素」について学ぶぞ。 元素は大まかに金属元素と非金属元素に分類される。金属元素とは簡単に説明すると陽イオンになりやすく、自由電子による金属結合をする元素のことです。身の回りにも金属製品はたくさんあるな。この金属元素には金属結合することで様々な金属なら . 第13族元素 - Wikipedia. 第13族元素(だいじゅうさんぞくげんそ)とは周期表において第13族に属する元素の総称。 ホウ素・アルミニウム・ガリウム・インジウム・タリウム・ニホニウムがこれに分類される。 ホウ素族元素とも呼ばれ、またホウ素をのぞいたアルミニウム・ガリウム・インジウム・タリウムを土類金属 . 両性 元素 と は質問箱 - Saitama U. スズ(Sn)と鉛(Pb)についてです.. 1,「スズと鉛は共に両性元素」と書いてある一文があったのですが,両性元素とはどのような元素のことですか?. 2,「鉛は,常温では塩酸や希硫酸に溶けにくい.これは,鉛の表面が冷水には溶けにくい塩化鉛,硫酸 . 金属粉(アルミニウム粉・亜鉛粉)│危険物取扱者になろう!. このように酸・アルカリの両方と反応するものを両性元素といい、アルミニウム・亜鉛・スズ・鉛の4つが該当します。 アルミニウム粉は反応性が高く、空気中の水分やハロゲン元素と反応して発火する危険があります。 保管方法.